Téknologi sintésis sapertos péptida
Panaliti sareng pamekaran ubar péptida ngembang pesat dina ubar.Nanging, pamekaran ubar péptida diwatesan ku ciri sorangan.Contona, alatan sensitipitas husus ka hidrolisis énzimatik, stabilitas diréduksi, sarta variability tina konformasi steric ngakibatkeun spésifisitas targeting low, hidrofobik low, sarta kurangna sistem angkutan husus.Dina raraga nungkulan péptida ieu, diusulkeun loba solusi jeung aplikasi suksés hiji jenis péptida mangrupa salah sahijina.
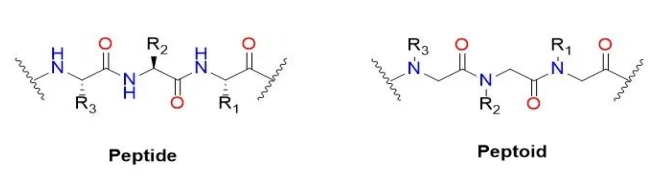
Jenis péptida (ngaran basa Inggris: Peptoid) atawa Poly – N – tinimbang glisin (ngaran basa Inggris: Poly real – N – substitutedglycine), nya éta sanyawa péptida kuasi péptida dina ranté utama.Ranté sisi karbon alfa mindahkeun ranté nitrogén utama tinimbang ranté samping.Dina polipéptida aslina, gugus R tina ranté samping asam amino ngagambarkeun 20 asam amino béda, tapi gugus R boga leuwih pilihan dina peptoid nu.Dina péptida, péptida dina ranté utama asam amino dina alfa karbon nitrogén tinimbang ranté samping mindahkeun kana ranté utama.Perlu disebatkeun yén péptida sacara umum henteu ngahasilkeun struktur maréntahkeun tingkat luhur anu sami sareng struktur sékundér dina péptida sareng protéin kusabab kurangna hidrogén dina nitrogén tulang tonggong.Tujuan awal péptida nyaéta pikeun ngembangkeun péptida anu stabil sareng protease tina ubar molekul leutik.
Analisis téhnik sintésis péptida-kawas
Métode sintésis péptida diwanohkeun
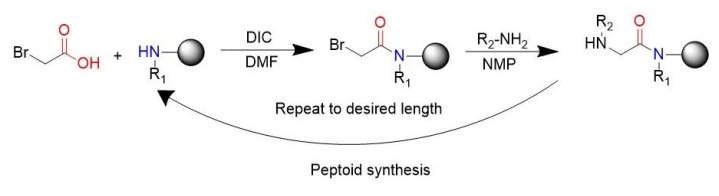
Métode sintésis kawas péptida umumna populér nyaéta métode sintésis subsingle invented by RonZuckermann, nu masing-masing dibagi jadi dua hambalan: acylation jeung kapindahan.Dina asilasi, lengkah kahiji nyaéta ngaktifkeun asam haloasetat pikeun ngaréaksikeun jeung amina sésa dina tungtung léngkah saméméhna, biasana diisopropil karbonisasi diimin.bromoaceticacid diaktipkeun ku diisopropylcarbodiimide."Dina réaksi substitusi (réaksi substitusi nukléofilik bimolekul), amina, ilaharna primér, nyerang halogén alternatif pikeun ngabentuk glisin N-substitusi.Jalur sintétik subunitér ngagunakeun amina primér anu sayogi pikeun ngahasilkeun péptida, ku kituna ngamungkinkeun sintésis kimia péptida.
Ekstensi padet dina sintésis péptida kelas gaduh pangalaman anu beunghar, tiasa nyayogikeun anjeun sababaraha jinis jasa sintésis péptida.
Analisis téhnik sintésis péptida-kawas
Kauntungannana péptida sapertos kitu
Leuwih stabil: péptoid leuwih stabil dina vivo ti péptida.
Selektipitas langkung: Peptoid cocog pisan pikeun panilitian penemuan ubar gabungan sabab rupa-rupa blok wangunan polipéptida anu béda tiasa didapet ku modifikasi gugus amino tulang tonggong.
Leuwih efisien: Kelimpahan struktur peptoid bisa nyieun peptoid pilihan alus pikeun metodologi scanning pikeun gancang manggihan struktur husus nu ngabeungkeut protéin.
Langkung poténsi pasar: ciri tina jenis péptida hayu eta jadi jenis ngembangkeun ubar boga poténsi hébat.
waktos pos: Dec-07-2023